Gary Ruot padece una enfermedad degenerativa sin cura y no cumplía la edad para entrar en el ensayo clínico con una terapia génica experimental. Su familia y amigos lo han conseguido
 Foto: Gary Ruot participa en un ensayo clínico para un tratamiento génico para intentar salvar su visión de la enfermedad degenerativa que padece. Crédito: Familia Ruot.
Foto: Gary Ruot participa en un ensayo clínico para un tratamiento génico para intentar salvar su visión de la enfermedad degenerativa que padece. Crédito: Familia Ruot.
La semana pasada, tras más de seis meses de espera, Gary Ruot de 17 años de edad, fue admitido en un ensayo clínico para probar un novedoso tratamiento para una rara enfermedad ocular degenerativa que se desarrolla deprisa y provoca una ceguera irreversible.
Se trata de una terapia génica. Los tratamientos de este tipo tratan de ralentizar o revertir una enfermedad hereditaria al introducir un gen sano donde se encuentra la versión mutada responsable de la enfermedad. Tras años de reveses, incluida la muerte de un paciente de 18 años de edad en un ensayo experimental en 1999, la terapia génica está viviendo un importante renacer para tratar enfermedades como la hemofilia, trastornos inmunes y enfermedades oculares degenerativas. Varios pequeños ensayos están generando resultados prometedores. Y mientras que aún hay riesgos, algunos pacientes no disponen de ninguna alternativa a estas terapias experimentales. Para esos pacientes, participar en un ensayo como este puede ser la diferencia entre curarse y seguir enfermos.
El problema es que el sistema tradicional de ensayos clínicos no iguala la urgencia a la que se enfrentan pacientes como Gary. Para lograr entrar en un ensayo clínico para una terapia génica, los pacientes han de cumplir con unos criterios específicos fijados por las farmacéuticas. Entre otras cosas, deben estar en un rango específico de edades y deben haber padecido los síntomas durante un período definido de tiempo. Gary tuvo la suerte de solicitar un cambio de las reglas de admisión de un ensayo para poder entrar. Pero muchas otras personas no son tan afortunadas.
En el caso de Gary, había poco margen para actuar. Su visión empezó a degenerarse en diciembre de 2015. En enero, dejó de jugar al baloncesto, y para febrero ya no veía lo suficiente para conducir. Ese mes fue diagnosticado con neuropatía óptica hereditaria de Leber (NOHL), una enfermedad que afecta a tan sólo una entre 50.000 personas a nivel mundial.
"Es un trastorno devastador que no tiene ninguna terapia eficaz", afirma la principal investigadora del ensayo, Nancy Newman, que también es profesora de oftalmología de la Facultad de Medicina de la Universidad de Emory (EEUU), uno de los emplazamientos del ensayo. "Por eso un paciente estará dispuesto a desplazarse al área de terapia génica, a pesar del hecho de que siempre habrá riesgos".
La madre de Gary, Jennifer Ruot, localizó el ensayo, que está siendo patrocinado por GenSight Biologics. Puesto que prueba un fármaco dirigido a corregir la mutación genética responsable de la pérdida de visión de Gary, era su mejor opción para recuperar la visión. Pero no podría ser admitido porque la edad mínima era de 18 años. Un amigo suyo creó una petición para que la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) redujera la limitación de edad. Jennifer llamaba y enviaba correos electrónicos a GenSight continuamente pidiendo datos actualizados del ensayo.
A veces la FDA necesita resultados positivos de seguridad en adultos antes de admitir niños. Este fue el caso de GenSight, que recibió este mes la aprobación regulatoria para admitir pacientes de entre 15 y 18 años.
GenSight fue capaz de aumentar ligeramente la población de pacientes para su ensayo porque NOHL es biológicamente la misma enfermedad en un paciente de 15 años que en uno de 20 años, según Newman. Algunos ensayos con terapias génicas están específicamente dirigidos a enfermedades en niños o incluso bebés. Pero no todas las terapias génicas se consideran seguras para los niños porque podrían dañar órganos que aún no hayan terminado de desarrollarse.
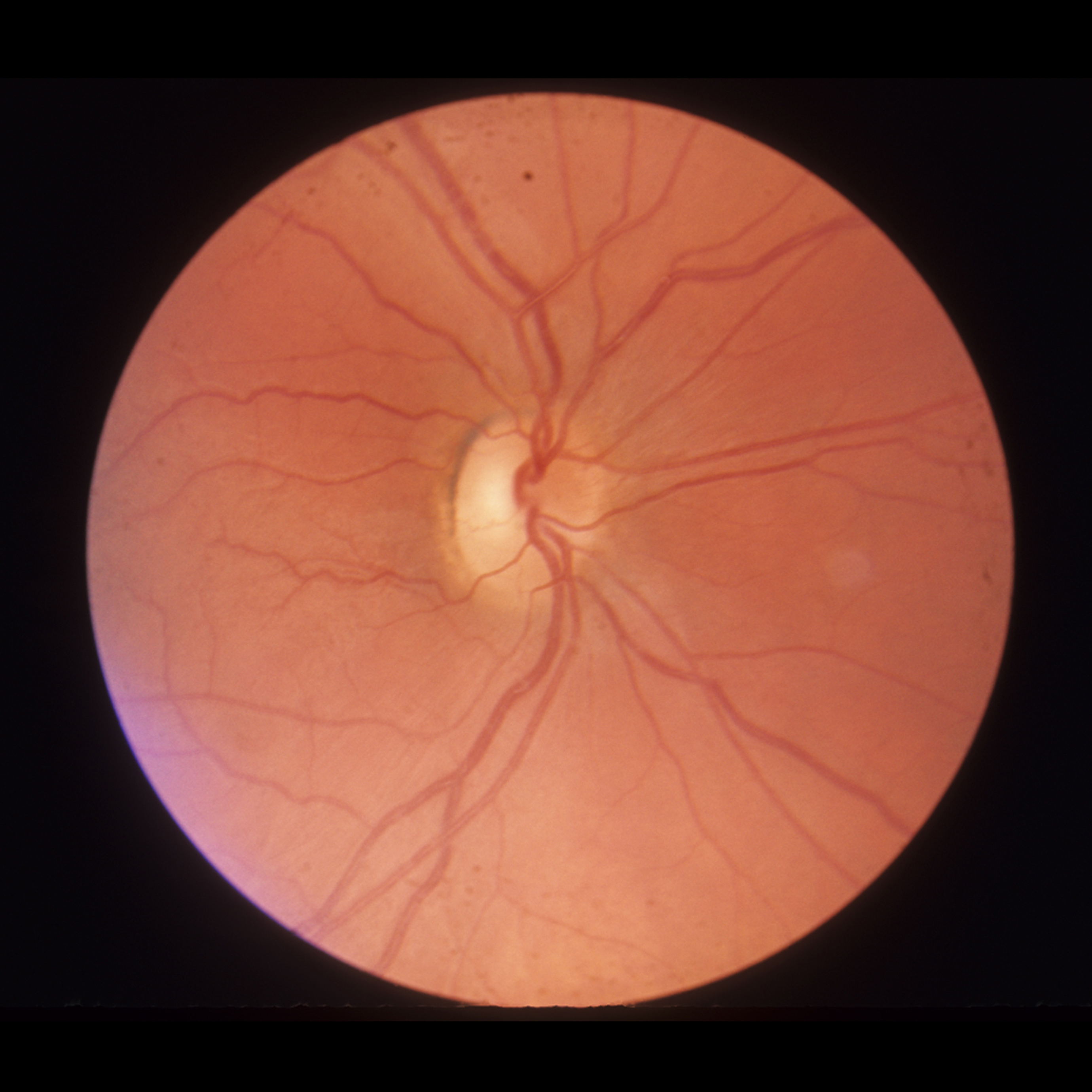
 Foto: Una imagen de un ojo con neuropatía óptica hereditaria de Leber. Crédito: Universidad de Arizona.
Foto: Una imagen de un ojo con neuropatía óptica hereditaria de Leber. Crédito: Universidad de Arizona.
Diseñar ensayos clínicos para terapias génicas es complicado. En las fases I y II, que intentan establecer la seguridad, los investigadores buscan pacientes con casos avanzados de la enfermedad. Eso minimiza los riesgos en caso de salir mal. Una vez que una terapia llega a la fase más avanzada, admite a pacientes que han desarrollado los síntomas más recientemente. Estudiar a estos pacientes es una mejor manera de medir la eficacia. Pero buscar pacientes en distintas fases de la enfermedad reduce la bolsa de los que finalmente podrán participar.
Gary fue especialmente afortunado. Los dos ensayos de GenSight para la NOHL sólo están admitiendo pacientes cuyos síntomas aparecieron el año pasado, por lo que pasó el corte por tan sólo un par de meses.
No todos los pacientes tienen tanta suerte. Algunas organizaciones están interviniendo para ayudar a conectar a los investigadores de terapias génicas faltos de sujetos de ensayo con pacientes que buscan desesperadamente mitigar una enfermedad devastadora. Por ejemplo, la Fundación Combatiendo la Ceguera, en Baltimore (EEUU), tiene un registro al que los pacientes pueden subir su información genética para ser emparejados con ensayos clínicos.
El director de comunicaciones científicas de la Fundación Combatiendo la Ceguera, Ben Shaberman, explica: "Si te dedicas a reemplazar genes necesitas encontrar a gente con ese gen mutado. Esa población puede variar desde un par de docenas de personas en todo el mundo hasta miles de ellas". Más de 250 mutaciones conocidas pueden causar enfermedades retinales heredetarias, por ejemplo.
La Alianza para la Medicina Regenerativa, una organización radicada en Washington D.C. (EEUU) que promociona terapias regenerativas y génicas, creó un comité especial en abril en parte para ayudar a guiar a los pacientes hacia los ensayos de terapias génicas.
Con la terapia génica a punto de realizar la transición desde idea hasta producto, muchos más pacientes podrán beneficiarse, por lo que se generará una necesidad aún mayor de apoyo. Aunque Gary y su familia puede que hayan logrado la mejor opción, aún no saben si la terapia de GenSight dará resultado, ni cuáles podrían ser los efectos secundarios.
Eso no parece preocuparle a Gary. El joven concluye: "Es algo de una sola vez, y representa una oportunidad para mejorar mi vida".