Al haber menos pacientes, las farmacéuticas podrían tener más poder para cobrar lo que quieran. Lo que está claro es que el coste de las terapias génicas aprobadas hasta la fecha está claramente relacionado a la inversa con el número de enfermos que podrían beneficiarse de ellas
La terapia génica, que consiste en introducir nuevo material genético en el ADN de una persona, es una forma revolucionaria de tratar algunos de los síndromes más raros del mundo. Sin embargo, las compañías farmacéuticas han puesto precios astronómicos a estos tratamientos tan específicos. De hecho, los costes son tan altos que uno de ellos ya ha sido retirado del mercado en Europa, y el otro está teniendo problemas para atraer pacientes.
Un nuevo tratamiento aprobado la semana pasada podría cambiar la ecuación. Yescarta es el segundo ejemplo de terapia génica que modifica el ADN en las células inmunes de una persona para atacar el cáncer. Lo que diferencia a Yescarta del primero es que podría tratar a muchos más pacientes que el resto de terapias genéticas aprobadas hasta ahora.
Para ver si existe una relación entre el precio de una terapia génica y el número estimado de pacientes que la recibirán cada año, hemos representado esas cifras para las terapias genéticas aprobadas y otra pendiente de aprobación en EE. UU. y las que se han aprobado en Europa.
El socio gerente de la firma de consultoría de ciencias biológicas Trinity Partners Herman Sánchez explica que existe una correlación entre la población de pacientes y el precio de la terapia: cuanto menos pacientes potenciales hay, más costosos son los tratamientos. Como se puede ver en el gráfico, los precios oscilan entre los 373.000 dólares (casi 321.000 euros) y un millón de dólares (más de 860.000 euros), mientras que el número máximo de pacientes por año sólo llega a unos 7.500.
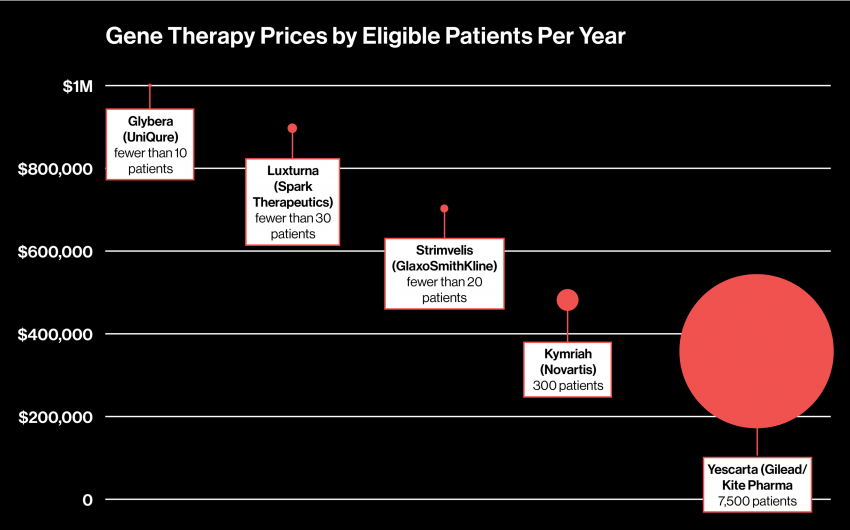
Gráfico: el precio de cada terapia génica está relacionado a la inversa con el número de pacientes potenciales a los que podría tratar. A mayor número de pacientes, menor precio. Las cifras de pacientes de Kymriah y Yescarta fueron proporcionados por Novartis y Gilead, respectivamente. Las poblaciones de pacientes potenciales para las otras terapias son estimaciones basadas en nuestros cálculos según la incidencia de la enfermedad.
Sánchez detalla: "Las enfermedades menos comunes tienen más poder para fijar los precios en el mercado. Esto se debe generalmente a que quienes los financian no tienen que lidiar con muchos pacientes".
De momento, Yescarta representa un valor atípico. Podría ayudar a unas 7.500 personas, según Gilead, el gigante de la biotecnología que adquirió al fabricante del medicamento, Kite Pharma, en agosto.Compare esa cifra con los pequeños grupos objetivo de las dos terapias genéticas aprobadas en Europa, Glybera y Strimvelis. Mientras tanto, en EE. UU., Novartis estima que alrededor de 300 pacientes al año serán aptos para su terapia genética Kymriah, que trata un tipo de leucemia infantil. Al tener más pacientes, Gilead fue capaz de establecer un precio más bajo, ya que al final podría obtener mayores ingresos totales.
A pesar de que el precio de Yescarta sigue provocando protestas entre los defensores de pacientes, es un buen precedente para las terapias genéticas en desarrollo destinadas enfermedades con más pacientes, como la hemofilia y la drepanocitosis, que afectan a unas 20.000 personas y 100.000 en EE. UU., respectivamente.
Si la enfermedad objetivo es más común, "habrá más presión sobre los precios", señala Sánchez.
La siguiente terapia genética pendiente de aprobación en EE. UU. se llama Luxturna, y devuelve una parte de la visión a pacientes de un tipo hereditario de ceguera. A principios de este mes, un panel de expertos independientes recomendó de forma unánime que la Administración de Alimentos y Medicamentos de EE. UU. debía aprobar Luxturna, fabricada por Spark Therapeutics. La agencia tomará su decisión antes del 12 de enero.
Spark calcula que entre 1.000 y 2.000 personas en EE. UU. podrían ser aptas para su terapia, que mejora la vista al reemplazar un gen mutado en las células de la retina. La compañía no quiso hacer estimaciones sobre cuántos pacientes podría tratar cada año, por lo que nuestras cifras se basan en la incidencia estimada de la forma de ceguera que trata Luxturna. Los analistas calculan que la terapia podría costar entre 800.000 dólares (más de 688.000 euros) y un millón de dólares (más de 860.000 euros) para tratar ambos ojos.
¿Qué implicaciones tiene todo esto para las compañías, las aseguradoras y los pacientes? Las empresas como Spark se enfrentarán a un dilema de precios cuando sus terapias obtengan la aprobación regulatoria. De momento, las aseguradoras en EE. UU. no han decidido si los cubrirán. Mientras tanto, los pacientes con afecciones médicas graves esperan no tener que pagar por los tratamientos.